암과 치료제의 최적 매칭
AI가 알려준다

AI(인공지능)를 활용한 신약 개발이 대세가 됐다. AI를 활용하면 신약 개발에 들어가는 막대한 기간과 비용을 감소시킬 수 있으며, 약물 상호 작용 등을 예측해 임상시험 설계 단계에서 나타나는 시행착오를 줄일 수 있다.
차백신연구소는 최근 목암생명과학연구소의 AI 알고리즘을 활용, 면역항암제 후보물질인 CVI-CT-001이 어떻게 암세포를 죽이는지를 규명하며 면역항암제 개발에 속도를 내고 있다.
특정 암에서 활성산소 유도 메커니즘 확인
이번 연구에서 차백신연구소는 CVI-CT-001이 세포에서 어떤 반응을 보이는지 확인하기 위해 목암생명과학연구소의 AI 알고리즘을 활용해 데이터를 분석했다. 차백신연구소가 실험의 디자인과 데이터 생산을 담당하고, 목암생명과학연구소는 AI 및 생명정보학 기술을 이용해 데이터를 분석하는 방식으로 협력했다.
실험에서 전립선암과 대장암, 그리고 면역세포인 대식세포까지 세 가지 세포주에 CVI-CT-001을 처리했다. 그 다음 AI 알고리즘을 활용해 CVI-CT-001이 어떤 경로를 거쳐 암 세포를 사멸하는지 살펴봤다.
전립선암 세포주에서는 암 세포가 사멸했다. 전립선암은 TLR2/3 발현이 높은 특징이 있다. CVI-CT-001이 전립선암의 TLR 연관 세포신호 전달체계를 활성화한 다음, 활성산소(ROS) 발생경로를 유도한 것을 확인했다. 이렇게 생성된 활성산소가 암 세포를 사멸시킨 것이다.
반면 대장암에서는 암 세포가 사멸하지 않았다. 대장암은 TLR2/3 발현이 낮다. 그래서 TLR 연관 세포신호 전달체계가 활성화되지 않아 활성산소가 발생하지 않았다. 대식세포는 TLR에 의해 활성화되는 만큼, CVI-CT-001 처리 후 TLR 세포신호 전달체계는 활성화됐다. 그러나 ROS 활성경로를 유도하지 않아, 세포 사멸로 이어지지 않았다.
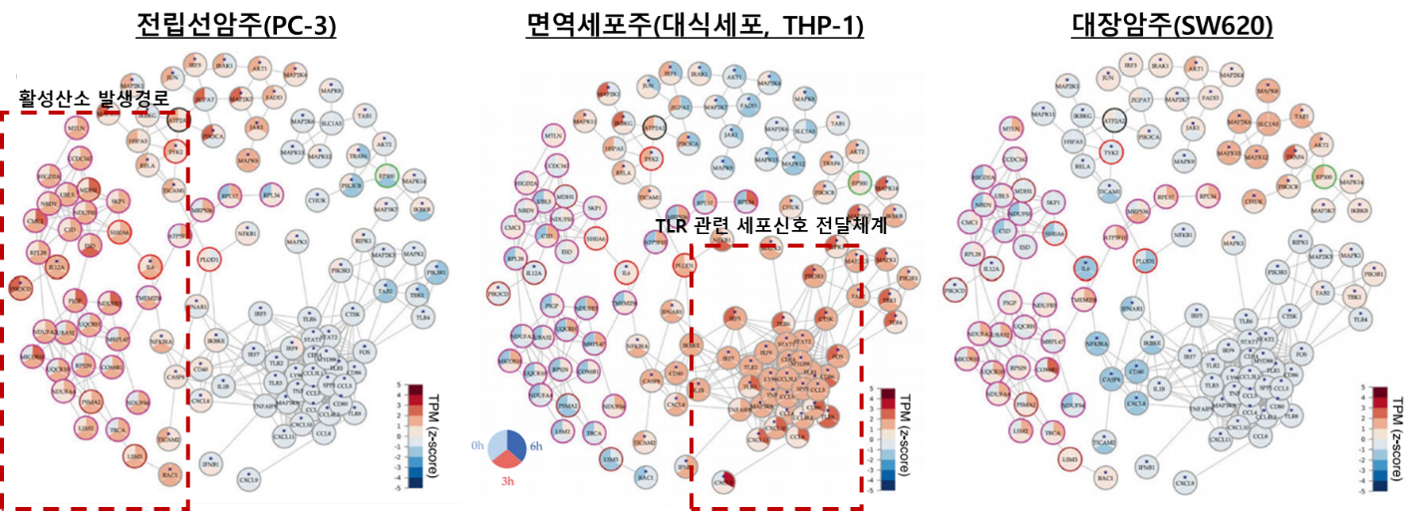
<세 가지 세포주에서 특정 유전자 모듈들 간의 서브 네트워크를 시각화하고 모듈 별 상대적 발현의 차이를 정량화한 분석도. (좌) 전립선암은 활성산소 발생경로가 활성화됐다. (중) 면역세포주는 TLR 관련 세포신호 전달체계는 활성화됐으나, 활성산소 발생경로까지 이어지지 않았다. (우) 대장암은 TLR 관련 세포신호 전달체계가 활성화되지 않았다.>
타깃 후보물질 발굴과 병용요법 전략 수립에 기여
이번 연구로 CVI-CT-001의 암 세포 사멸 기전에 대한 중요한 단서를 확인하면서, 면역관문억제제와 병용요법으로 암을 치료할 수 있는 가능성이 충분하다는 것을 입증했다.
3세대 면역항암제인 면역관문억제제는 암 세포가 면역체계를 회피하는 것을 억제하여 우리 몸의 면역세포가 암세포를 공격하게 한다. 세포 독성이 적어 기존 항암제보다 부작용이 작다. 반면 종양 내 환경에 면역세포가 극히 적거나, 침투하지 못하는 ‘저면역원성(콜드 튜머·Cold Tumor)’ 상태에서는 치료 반응률이 30%에 불과하다는 한계가 있다.
CVI-CT-001은 차백신연구소가 독자개발한 면역증강제 ‘엘-팜포(L-pampoTM)’를 활용한 면역항암제 후보물질이다. L-pampo™는 TLR2와 TLR3 리간드(수용체에 특이적으로 결합하는 물질)의 복합체다. 우리 몸의 선천성 면역에 관여하는 세포 내 단백질인 TLR를 자극해 체내 면역세포를 활성화해 면역반응을 유도한다. 백신제형으로 사용될 때는 항원의 면역원성을 높여준다. 면역항암제로 사용될 때는 암 세포의 사멸을 유도하고 종양미세환경을 저면역원성에서 고면역원성으로 조성하는 역할을 한다.
CVI-CT-001은 전임상연구에서 특정 암세포를 사멸시키고 암세포 내의 환경을 고면역원성으로 전환한다는 점을 확인한 바 있다. 2024년 4월 미국암연구학회(AACR)에서 발표한 전임상 결과에 따르면 CVI-CT-001을 단독으로 투여한 대장암 모델에서 종양이 83.7% 감소한 반면, 2개의 면역관문억제제를 각각 투여한 모델에서는 17.3%와 23.6%만 감소했다. CVI-CT-001과 면역관문억제제를 병용으로 투여했을 때는 종양이 96.6% 감소했다. CVI-CT-001을 투여할 경우, 암세포 사멸에 중요한 역할을 하는 킬러 T세포도 증가했다.
이러한 임상 결과를 AI 알고리즘으로 확인한 것이 이번 연구의 성과다. 항암제 개발에서 중요한 것은 치료물질이 어떻게 암세포에 작용하는지 그 기전을 규명하는 것이다. 암 세포 종류가 다양하고, 각각의 암마다 종양 내 환경이 복잡하고 다양해 치료물질이 어떻게 작용하는지 파악하기 쉽지 않다.
이번 연구에서 AI를 활용해 암 세포 사멸 유도 기전을 예측한 만큼, 차백신연구소는 항암제 후보물질이 어떤 암에 더 잘 작용하는지, 병용 요법에서 어떤 점을 보완할지 전략을 수립하는데 도임이 될 것으로 기대하고 있다.
<차백신연구소 연구원이 AACR 2024 참가자에게 CVI-CT-001 전임상 결과를 설명하고 있다>
항암제 후보물질 발굴, 백신 효과 개선도 기대
차백신연구소는 AI를 활용한 파이프라인을 구축하는데 힘을 기울이고 있다. 빅데이터 및 AI 기술 기반 신약개발 기업인 파로스아이바이오와 협약을 맺고 AI 기반의 신약 후보물질 발굴에 주력하고 있다. AI를 사용하면 시판 중인 약물을 다른 적응증(질환)의 신약으로 사용하는 ‘약물재창출(Drug Repositioning)’을 수월하게 할 수 있어, 그만큼 신약 개발에 들어가는 비용과 시간을 단축할 수 있다.

차백신연구소가 보유한 백신을 개량하는 것에도 AI를 활용할 수 있다. 현재 만성 B형간염 치료백신(CVI-HBV-002), B형간염 예방백신(CVI-HBV-001), 대상포진백신(CVI-VZV-001) 등 백신 파이프라인을 보유하고 있다. AI를 활용하면 이러한 백신의 효과를 더 끌어올리거나, 아예 새로운 백신으로 개발할 수 있다. #
관련 기사 이어서 보기 → 차백신연구소-목암생명과학연구소 AI 활용해 면역항암제 후보물질의 새로운 항암 기전 규명










