판 커지는 세포·유전자치료제
‘벡터 CDMO’도 뜬다

세포·유전자치료제(Cell and Gene Therapy; CGT)가 기존 치료법으로는 해결할 수 없는 미충족 의료 수요를 충족시킬 차세대 기술로 주목받고 있다. 유전자와 세포를 직접 수정하거나 조작해 질병의 근본 원인을 치료하는 방식이다.
2020년 출시된 노바티스(Novartis)의 유전자치료제 졸겐스마(Zolgensma)는 출시 1년 만에 매출 1조원을 돌파해 업계를 놀라게 했다. 유전자 돌연변이로 근육이 악화되거나 소실되는 척수성근위축증을 치료하는 데 사용되는 이 약의 가격은 약 28억원이다. 비싼 가격에도 불구하고 매년 수요가 폭증하고 있다.

한국보건산업진흥원이 발표한 ‘글로벌 시장 전망 및 오픈 이노베이션 동향’ 보고서에 따르면, 글로벌 CGT 시장은 2021년 기준 약 74억7000만 달러(9조7600억원)이며 오는 2026년 555억90만 달러(72조5300억원) 규모로 예상된다. 연평균 성장률은 49.1%에 달한다.
CGT 시장이 성장함에 따라 바이럴 벡터(viral vector) 위탁개발생산(CDMO) 수요도 급증할 전망이다. 바이럴 벡터는 유전물질을 전달하는 물질로, 유전자치료제 개발에 필수적인 요소다. 바이럴 벡터는 문제가 생긴 유전자를 보충하거나 대체하는 용도로, AAV(adeno-associated virus, 아데노 연관 바이러스)나 LV(Lentivirus, 렌티바이러스) 등이 주로 사용된다.
바이럴 벡터 시장 선점한 해외 CDMO 기업
유전자치료제에 사용되는 바이럴 벡터 중 시장을 주도하는 것은 AAV다. 노바티스의 척수성근위축증 치료제 ‘졸겐스마’, 유전성 망막질환 치료제 ‘럭스터나(Luxturna)’ 등의 매출이 성장하며 시장 규모가 커지고 있다. AAV 벡터를 사용해 임상 중인 치료제 후보물질은 300여개에 이르고 있어 앞으로 시장이 더 커지고 다양화될 것으로 보인다.

이에 따라 AAV 벡터를 타깃으로 하는 CDMO 기업도 주목받고 있다. 해외 기업 중 미국의 찰스 리버(Chales river), 카탈렌트(Catalent), 바이럴진(Viralgen), 써모피셔 사이언티픽(Thermo Fisher Scientic), 중국의 우시 앱텍(Wuxi AppTec) 등이 있다.
찰스 리버는 인수합병을 통해 AAV 벡터 포함한 유전자치료제 CDMO 서비스를 구축했다. 2021년 세포치료제 CDMO 기업인 코그네이트 바이오서비스(Cognate BioServices)를 8억7500만 달러, 바이러스 벡터 제조 전문 기업인 비젠 바이오사이언스(Vigene Bioscience)를 3억5000만 달러에 각각 인수했다.
카탈렌트 역시 2019년 AAV와 LV 벡터 제조 전문 기업 파라곤 바이오서비스(Paragon Bioservices)를 12억 달러에 인수해 관련 서비스를 구축했다. 볼티모어와 워싱턴 2곳의 시설에서 AAV 벡터 공정과 CAR-T 등 면역세포치료제 LV 공정 서비스를 제공하고 있다. 2022년에는 AAV 벡터 제조 공정 속도 향상을 위한 플랫폼 ‘Uptempo Virtuoso‘를 공개하기도 했다.
바이럴진은 유전자치료제 전문 기업 애스크바이오(AskBio)의 CDMO 사업을 담당하고 있는 자회사다. 2020년 애스크 바이오가 다국적제약회사 바이엘(Bayer)에 인수되면서 자연스레 바이엘 산하로 편입되어 바이엘의 바이럴 벡터 CDMO 사업을 담당하고 있다. 바이럴진은 8,300만 달러를 들여 스페인 스페인 최초의 유전자 치료제 생산시설을 스페인 산세바스티안(San Sebastian)에 구축했다.
써모피셔 사이언티픽은 2017년 CDMO 서비스 전문 기업 파테온(Patheon)을 72억 달러에 인수한 다음, 2019년 AAV 치료제 생산 서비스를 주요 사업으로 하는 바이럴 벡터전문 CDMO 기업 브래머 바이오(Brammer Bio)를 17억 달러에 인수했다. 브래머 바이오는 미국 메사추세츠주에 상업용 cGMP 바이러스 벡터 제조 시설을 보유하고 있다. 써모피셔 사이언티픽는 브래머 바이오를 파테온으로 편입시킴으로써 파테온의 바이럴 벡터 생산 규모를 늘리며 서비스를 제공하고 있다.
우시 앱텍은 2020년 AAV 벡터 서스펜션 플랫폼(XAAV)을 론칭하면서 AAV 벡터 배양 및 품질분석 서비스를 개시했다. 2021년에는 영국 AAV 벡터 제조 업체 옥스진(Oxgene)을 인수해 우시 어드밴스드 테라 피스 자회사로 편입시켰다. 옥스진의 AAV 생산 세포주 개발 기술 및 공정 플랫폼 기술이 결합한 AAV 벡터 제조 플랫폼 TESSA를 바탕으로 고객 맞춤형 AAV 공정 및 생산을 서비스하고 있다.
K-바이오, 바이럴 벡터 개발 경쟁 본격화
국내 바이오 기업들도 바이럴 벡터 기술 역량을 갖추기 위해 노력하고 있다.
항암 AV(Adenovirus, 아데노바이러스) 신약개발을 목표로 설립된 진메디신은 2022년 8월 경기 하남시에 4300㎡(약 1300평) 규모의 바이럴 벡터 GMP 설비를 갖춘 공장을 완공했다. 바이럴 벡터 전문 CDMO 설비로는 국내 최대 규모로 알려져 있다. AV, AVV, LV, HV(Herpes virus, 헤르페스 바이러스) 등 6종의 주요 바이럴 벡터를 생산할 수 있다.
씨드모젠은 다양한 바이러스 전문 의약품 GMP 시설을 보유한 바이오벤처다. 비임상시험용 소량생산부터 초기 임상시험에 필요한 AV 벡터를 생산하고 있다. 2020년 미국의 바이러스 전문제제 개발 기업 VSI(Vaccine Stabilization Institute)와 업무협약을 체결하고 바이럴 벡터의 공정개발, 분석법 개발 등을 공동으로 추진하고 있다.
이연제약은 2017년부터 2021년까지 800억원을 투자해 유전자치료제 원스톱 생산시설인 충주 바이오공장을 준공했다. 50L, 200L 멀티 유즈(Multi-Use) 배양기와 싱글 유즈(Single-Use) 30L, 50L, 500L 배양기를 확보해 AVV를 생산하는데 필요한 원료인 플라스미드 DNA 생산 역량을 갖추고 있다. 유전자치료제 개발 전문기업 뉴라클제네틱스와 자체 생산한 AVV 벡터를 활용해 습성 노인성 황반변성 치료제를 개발하고 있다.
첨단바이오의약품 신약개발 전문기업 이엔셀은 세포와 바이럴 벡터를 동시에 생산할 수 있는 GMP 시설을 구축해 국내에서 유일한 원스톱 서비스를 제공하고 있다. 노바티스의 킴리아(Kymriah) 및 얀센(Janssen)의 카비티(Carvykti) 등 키메릭 항원 수용체 T-세포(CAR-T) 계열 치료제의 중앙세포처리센터로 지정되기도 했다. 회사가 현재까지 수주한 금액은 2024년 8월 기준 모두 380억원으로 국내에서 CGT CDMO 시장에서 국내 1위 매출을 기록하고 있다.
글로벌 제약·바이오 기업들이 암·유전 질환을 넘어 다양한 질환에 CGT 개발이 이어지고 있지만 국내에선 이를 따라가지 못하고 있다. 전세계 CGT 개발 기업은 1천 457개인데, 이 중 47.1%인 686개가 북미에 소재하고 있다. CDMO도 마찬가지다. 글로벌 시장조사기관 프로스트&설리번 (Frost & Sullivan)에 따르면 바이오의약품 CDMO 매출 중 북미 매출이 94억2천만억 달러로 전체 47.8%를 차지했다. 그만큼 생존을 위해서는 북미 시장 진출이 무엇보다 중요하다.
SK그룹의 원료의약품 위탁개발생산 자회사인 SK팜테코는 2023년 미국 CGT CDMO 업체인 CBM(The Center for Breakthrough Medicine)을 인수하며 북미 CGT CDMO 시장에 진출했다. CBM은 세포·유전자 치료제 단일 생산시설 기준 세계 최대 규모인 6만5000㎡의 시설을 건설 중이며, 현재 이 중 약 2만8,000㎡를 완공해 바이럴 벡터 GMP 시설과 개발·분석 연구실을 운영하고 있다.
GC셀은 2022년 미국 CGT CDMO 기업 바이오센트릭 지분 100%를 인수하며 북미 시장 공략에 박차를 가했으며, 메디포스트도 같은 해 캐나다 CGT CDMO 기업인 옴니아바이오의 지분을 인수하는 등의 행보를 보이고 있다.
CGT 최대 시장 북미 지역 공략하는 차바이오텍
차바이오텍은 북미 CGT CDMO 시장 공략을 위해 자회사 마티카 바이오테크놀로지(이하 마티카 바이오)를 설립했다. 2022년 한국 기업으로는 유일하게 미국 텍사스주 칼리지스테이션에 CGT CDMO 시설을 준공했다.
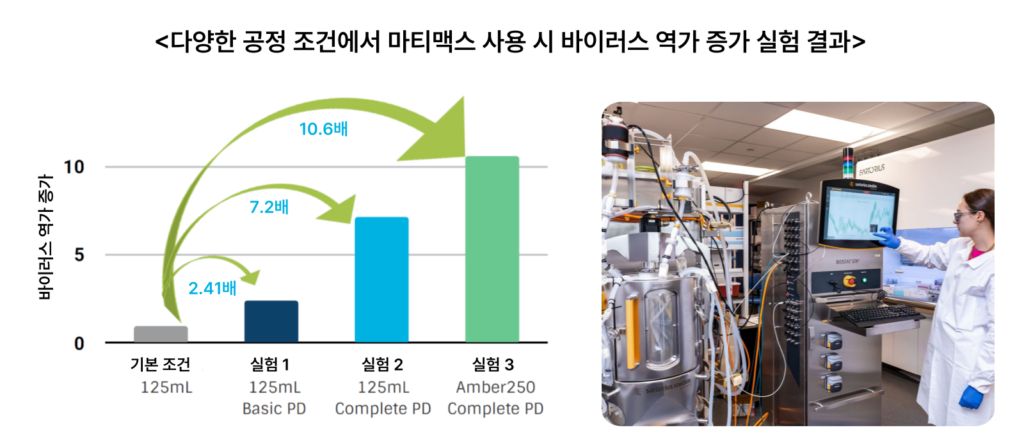
마티카 바이오의 장점은 바이럴 벡터 자체 기술력을 보유하고 있다는 점이다. 이 기술력을 토대로 AAV는 물론 LV, RV(Retrovirus Vector, 레트로바이러스) 등 다양한 바이럴 벡터 생산이 가능하다. 2023년에는 자체 세포주 ‘마티맥스(MatiMax™)’를 개발하며 바이럴 벡터 생산 효율을 더 높였다. 2024년에는 바이러스 캡시드(capsid) 분리 분석법을 자체 개발하며 바이럴 벡터 생산에 필요한 보다 정확한 데이터를 확보할 기술력을 갖췄다. 그 외에도 ‘실시간 공정 분석기술’과 ‘자동화 시스템’을 구축하며 바이럴 벡터의 대량 생산의 밑바탕을 마련 중이다.
생산 능력도 확대 중이다. 최근 2공장 확장을 결정하고 시설 투자를 위한 행정적 절차를 마무리했다. 2공장이 완공되면 현재 중∙소규모 임상시료 생산에 더하여 대용량 상업화 생산까지 역량이 확대될 예정이며, 이에 따라 의약품 개발에 필요한 모든 단계의 서비스를 제공할 수 있다.
마티카 바이오는 이러한 기반을 토대로 미국 내 600여개 CGT 개발사를 대상으로 제조시설 보유 여부, 파이프라인 종류 및 개수 등 다양한 요인을 내부적으로 분석해 계약이 가능한 개발사를 별도로 선정, 집중 공략하고 있다. 최근 잇단 수주 계약을 따내며 본격적인 궤도에 올랐다.

차바이오텍은 마티카 바이오를 포함한 글로벌 5개 사이트에 CGT CDMO 네트워크를 구축했다. 글로벌 5개 사이트 CGT CDMO 네트워크는 △바이럴벡터를 중심으로 CGT 공정 전문가가 포진해 있는 마티카 바이오 △분석 및 다양한 세포치료제 생산을 전문으로 하는 마티카바이오랩스 △CGT 분야에서 단일 시설로는 세계 최대 규모의 CGB(Cell Gene Biobank) △세계 최초로 병원내 GMP시설을 확립한 분당차병원 GMP △1만례 이상의 면역세포 및 줄기세포 치료 경험을 보유한 일본 마티카바이오재팬으로 구성된다.
차바이오텍은 경기도 성남시 판교 제2테크노밸리에 지상 10층, 지하 4층, 연면적 6만 6115㎡(2만평)으로 CGT 분야에서 단일 시설로는 세계 최대 규모인 CGB(Cell Gene Biobank)를 건설 중이다. CGB에는 CDMO 생산시설 및 cGMP(우수의약품생산규격) 제조시설, 줄기세포 바이오뱅크 등이 들어선다. CGT, 메신저리보핵산(mRNA), 바이럴벡터, 플라스미드 DNA를 한 건물에서 동시에 생산할 수 있게 된다. 미국 현지에 비해 저렴한 비용으로 고품질의 제품을 생산할 수 있을 것으로 기대된다.
각 사이트별 특장점을 공유하는 유기적인 운영을 통해 CGT를 개발하는 기업이 국내는 물론 글로벌로 진출할 수 있도록 각 기업 특성에 맞춰 CGT CDMO 서비스를 제공할 계획이다. 차바이오텍의 글로벌 5개 사이트 CGT CDMO 네트워크는 CGT 공정개발과 분석기술 등 최신 기술뿐만 아니라 각 사이트별 특장점을 공유하는 유기적인 운영을 통해 시너지를 발휘하게 된다. 고객사의 특성에 맞춰 CGT 개발부터 생산, 임상까지 원스톱 솔루션을 제공할 계획이다. 차바이오텍에 CDMO를 맡기는 기업은 5개 사이트 중 최적의 생산 거점을 선정해 제품을 생산함으로써 해당 국가 시장에 진출할 수 있다.
벡터 시장 확대 위해 넘어야 할 과제 많아
바이럴 벡터 유형에 대한 연구 개발은 각 유전자 치료제에 적합한 운반체의 선택의 폭을 넓혀주면서 희귀·난치성 질환의 치료 가능 영역을 확장시키고 있다. 하지만 바이럴 벡터 CDMO 시장이 확대되기 위해서는 넘어야할 과제도 존재한다.
바이럴 벡터는 아직 생산공정이 구체적으로 확립되어 있지 않아 균일한 품질의 제품을 생산하는데 어려움이 있다. 균일한 품질의 바이럴 벡터를 대량 생산하기 위해서는 실시간 공정데이터를 수집·분석하는 것이 매우 중요하다. 이에 따라 바이럴 벡터 CDMO 기업들은 고객이 원하는 맞춤형 공정 서비스와 그에 맞는 최적의 배양 프로토콜 정립 및 생산서비스까지 동시에 이뤄지는 CRO+CDMO 결합형 통합 솔루션을 제공하는 것이 최종적인 목표가 될 수도 있다. 마티카 바이오가 캡시드 분리 분석법을 자체 개발하고, 공정 분석기술을 개발하는 것도 이러한 일환이다.

<마티카 바이오는 글로벌 바이오공정 전문기업인 싸토리우스社와 실시간 공정분석기술과 자동화 시스템을 개발하고 있다.>
바이럴 벡터 자체의 한계를 극복하는 것도 필요하다. 대표적인 것이 바이러스 용량을 감소시키는 것이다. 고용량 바이러스 사용은 크게 두 가지 문제가 있다. 먼저 안전성 문제다. 전신 치료에 사용되는 유전자치료제는 고용량 바이러스를 투여하게 되는데, 이 때 체내 세포 수의 몇 배에 달하는 양이 투입되는 경우가 있다. 이로 인해 부작용이 발생할 수 있다.
다량의 바이럴 벡터 제조 시 비용적인 문제도 있다. 일례로 AAV 벡터는 일반적인 생산 단가 기준 표준 용량 당 약 10만 달러 정도인데, 이렇게 생산된 바이럴 벡터로 만들 수 있는 유전자 치료제는 약 10회 분에 불과하다. 여기에 대부분의 유전자치료제가 희귀질환에 사용되어 환자 수가 매우 적다는 점, 그리고 치료법 개발에 투자된 비용 등이 더해져 가격이 비쌀 수밖에 없다. 가장 비싼 유전자 치료제인 ‘헴제닉스’의 1회 투약 비용은 350만 달러(한화 약 42억 8050만 원)이다. 노바티스의 척수성근위축증 치료제 ‘졸겐스마’ 역시 210만 달러(한화 약 29억원), 블루버드 바이오의 지중해빈혈 치료제 ‘진테글로’는 280만 달러(한화 약 37억원)에 달한다. #









